Las fórmulas orgánicas
La fórmula de los compuestos orgánicos es, coloquialmente hablando, un código en el que se puede ver de manera rápida y sencilla el número de átomos que forma un determinado compuesto.
En la mayoría de los casos, esta fórmula molecular nos aporta poca información, ya que existen ciertos compuestos orgánicos diferentes con la misma fórmula molecular. Esto se debe a que con el mismo número de determinados átomos se pueden formar diferentes enlaces, creando moléculas geométricamente diferentes y con características diferentes.
Fórmulas en dos dimensiones
- Fórmula molecular

- Fórmula semidesarrollada

Se representan solo los enlaces entre los átomos de carbono y se indican los átomos unidos a estes.
- Fórmula desarrollada

- Fórmula mixta

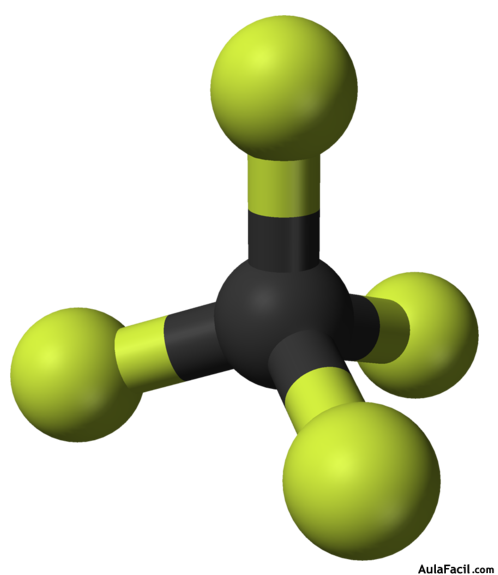
Representación tridimensional
Este tipo de representaciones permite obtener una imagen visual de su estructura espacial y apreciar la geometría del esqueleto de las moléculas.
El modelo de representación más real es el modelo compacto, pero a la hora de estudiar un compuesto normalmente el más usado es el de bolas o de varillas ya que se observa mejor la colocación de los átomos y sus enlaces.
- Modelo de bolas

- Modelo de varillas

- Modelo compacto

¿Cómo dibujar moléculas en cadena?
En un examen o ejercicio existen diversas maneras de presentar los compuestos. La más clara puede ser la fórmula desarrollada o mixta, pero esta suele ser muy extensa y demasiado explícita a un cierto nivel académico.
La manera correcta para dibujar compuestos es con un sistema de varillas, que puede ser plano o tridimensional. Esto dependerá del nivel y exigencia del profesor, así como el tipo de ejercicio que se esté planteando.
Cada punta de cada varilla indicará un carbono. Si no se indica concretamente a qué está enlazado ese carbono, siempre se supondrán tantos hidrógenos como enlaces pueda formar. De no ser un hidrógeno, deberá ser indicado.
Importante. Debido al ángulo que presentan los enlaces de carbono, la estructura de varillas se dibujará en zig-zag.
Ejemplo:

C5H12O
Ejercicios:

| 1) | ||
Corregir
Ver Solución
Limpiar | ||

| 1) | ||
Corregir
Ver Solución
Limpiar | ||

| 1) | ||
Corregir
Ver Solución
Limpiar | ||